
【澎湃新闻】生命科学
Life science
2026年3月19日,吉林大学魏伟教授课题组在Cell Press细胞出版社旗下期刊Cell Chemical Biology上发表了题为“Mechanosensation promotes broad-spectrum antiviral defense through membrane remodeling”的研究论文。该研究被期刊遴选为当期“精选文章”(Featured Article),并同期配发了题为“The membrane strikes back: A mechanical force awakens antiviral defense”的专家评述(Preview),对该成果进行了重点推介与深度解读。
该研究首次定义机械力介导抗病毒反应系统(MARS),揭示了细胞通过感知机械力刺激激活Piezo1离子通道,进而诱导细胞膜重塑,在物理层面构建起一道阻挡病毒入侵的广谱防线。研究不仅阐明了这一不依赖干扰素的天然免疫新机制,也为抗病毒治疗提供了全新的“物理疗法”策略。
病毒持续对全球公共卫生构成重大威胁。传统的抗病毒策略多针对病毒自身的蛋白或核酸进行设计,然而病毒极易发生突变以逃避药物攻击,导致耐药性问题频发。相比之下,宿主细胞如何主动感知环境并建立防御屏障的机制尚不完全清楚。细胞作为生命的基本单元,具备感知机械力并将其转化为生物信号的能力(即机械力传导)。既往研究表明,病毒感染过程本身会对细胞膜产生机械扰动,但细胞是否能主动利用机械力信号来对抗病毒,一直是未被探索的盲区。鉴于病毒入侵必须突破细胞膜这一物理屏障,探究机械力感知是否参与抗病毒防御具有重要的科学意义。
该研究团队以呼吸道肠道病毒EV-D68为模型,意外发现高细胞密度培养条件下的细胞对病毒感染表现出显著的抵抗力。通过系统的基因筛选与功能验证,研究者证实这种由细胞间机械挤压产生的“接触抑制”效应,依赖于机械力敏感离子通道Piezo1的激活。当细胞感受到机械压力时,Piezo1通道开放,触发下游信号通路,导致宿主细胞膜的流动性显著降低(即膜变“硬”)。由于病毒入侵高度依赖细胞膜的流动性来完成融合或内吞,这种膜性质的改变直接切断了病毒的进入途径。
进一步的研究表明,MARS系统具有惊人的广谱抗病毒特性。除了EV-D68,激活Piezo1还能有效抑制柯萨奇病毒、鼻病毒以及流感病毒等多种包膜和非包膜病毒的感染。更为重要的是,这种防御机制独立于传统的干扰素免疫系统,代表了一种古老的、基于物理屏障的先天免疫新形式。
在转化应用方面,研究团队展示了两种极具潜力的干预策略:一是使用Piezo1的小分子激动剂(如Yoda1)模拟机械力刺激,在体外细胞和类器官模型中均显示出强大的抗病毒效果;二是直接在体施加机械振动。在新生小鼠致死性EV-D68感染模型中,无论是注射Piezo1激动剂还是给予早期的机械振动处理,均能显著降低病毒载量,防止神经系统损伤,避免小鼠出现类似小儿麻痹症的后肢瘫痪,并提高了小鼠存活率。这一发现提示,物理治疗手段可能成为预防或治疗病毒感染的新选择。
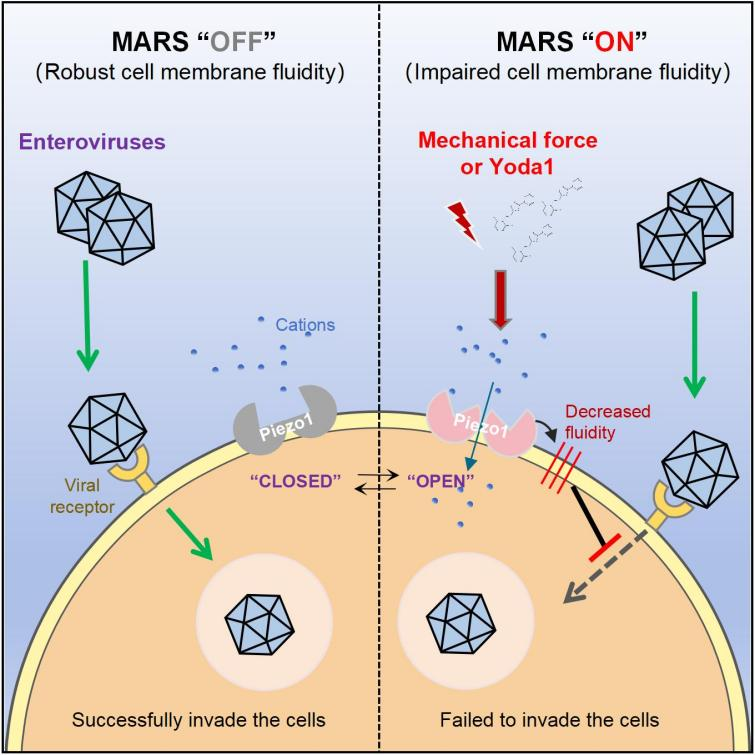
总的来说,本研究发现了宿主细胞感知机械力并转化为抗病毒信号的MARS系统,揭示了通过调节细胞膜物理性质来阻断病毒入侵的非经典免疫机制。该成果不仅拓展了人们对innate immunity的认知边界,将物理力学与免疫学紧密联系起来,更为开发不易产生耐药性的广谱抗病毒药物及物理治疗手段提供了新思路。
作者专访
Cell Press细胞出版社特别邀请本文通讯作者魏伟教授进行了专访,请他为大家进一步解读。
CellPress:
本文的研究亮点是什么?
魏伟教授:
本文最大的亮点在于我们发现了一种新的免疫防御模式—“力学免疫防御”。传统观念认为免疫主要靠化学信号(如细胞因子、抗体)来识别和清除病毒,而我们发现细胞通过“感受”物理压力,也能启动防御程序。具体来说,我们鉴定出Piezo1是这一过程的关键传感器,它被激活后会让宿主细胞膜重塑,像给细胞穿上了一层“防弹衣”,让病毒进不来。此外,我们证明了这种策略是广谱的,对多种呼吸道病毒都有效,这为抗病毒治疗打开了一扇全新的大门。
CellPress:
本文的科学意义是什么?
魏伟教授:
这项工作的科学意义在于它填补了先天免疫系统的一块重要拼图。过去我们知道有物理屏障(如皮肤)和化学屏障(如干扰素),现在MARS系统连接了这两者,表明物理刺激可以转化为生物学防御信号。这是一种不依赖病毒特异性识别的防御机制,因此病毒很难通过突变来逃逸。从进化角度看,这可能是一种古老且保守的生存机制。我们的研究将生物力学与病毒学和免疫学交叉融合,为理解宿主与病毒相互作用提供了新的物理学视角。
CellPress:
您团队未来对该项目后续有哪些研究计划?
魏伟教授:
未来我们将深入探索MARS系统在人体生理状态下的具体作用,例如日常运动产生的机械力是否天然增强了我们的抗病毒能力。另外,我们也在探索如何将机械振动疗法标准化,评估其在婴幼儿等特定人群中的安全性和有效性,希望能为那些缺乏特效药的病毒性传染病提供一种普惠的、低成本的物理防治方案。

作者介绍

魏伟
教授
魏伟,吉林大学第一医院教授、博士生导师,吉林大学唐敖庆学者领军教授,国家自然科学基金委优秀青年基金获得者,吉林大学艾滋病与病毒研究所副所长。课题组长期从事病毒元件与宿主互作研究,近5年以通讯作者(含共同)在Science、Cell Host &Microbe、Cell Chemical Biology、Science Signaling、Nature Communications、Cell Reports、EBioMedicine、EMBO Reports等期刊发表多篇学术论文。
相关论文信息
论文原文刊载于Cell Press细胞出版社
旗下期刊Cell Chemical Biology
▌论文标题:
Mechanosensation promotes broad-spectrum antiviral defense through membrane remodeling
▌论文网址:
https://www.sciencedirect.com/science/article/pii/S2451945626000243
▌DOI:
https://doi.org/10.1016/j.chembiol.2026.01.004
原标题:《吉林大学魏伟Cell Chemical Biology:发现机械力感应介导的抗病毒新机制 | Cell Press对话科学家》
 吉林大学召开领导班子树立和践行...04-05
吉林大学召开领导班子树立和践行...04-05 央视《焦点访谈》报道吉林大学第...04-05
央视《焦点访谈》报道吉林大学第...04-05 田辉到物理学院、化学学院调研04-03
田辉到物理学院、化学学院调研04-03 花开吉大 | 程立辉:用十二时辰守...04-03
花开吉大 | 程立辉:用十二时辰守...04-03 吉林大学刘雪莲教授文章入选中宣...04-02
吉林大学刘雪莲教授文章入选中宣...04-02 CCS Chemistry 2026年第4期主编寄...04-01
CCS Chemistry 2026年第4期主编寄...04-01 吉林大学召开领导班子树立和践行...03-31
吉林大学召开领导班子树立和践行...03-31 吉林大学举行2026年党员基本培训...03-31
吉林大学举行2026年党员基本培训...03-31


