【澎湃新闻】你在家刷视频、打电话、看导航,信号满格,干啥都顺溜。这就是脑子好使,记性好,反应快。
阿尔茨海默病后:信号越来越差。刚开始是卡顿,话到嘴边想不起来(忘事)。后来是掉线:刚说的话转头就忘,出门找不到路(迷路)。再最后,不认识人,不会说话,生活不能自理。
科学家一直在寻找更安全、更精准、能真正帮大脑清理垃圾并恢复认知的新方案。

2026年2月12日,吉林大学生命科学学院吴慧副教授在Brain Behavior and Immunity发表:Self-assembling ferritin nanoplatform enables amyloid-β-targeted immunotherapy and cognitive rescue in APP/PS1 mice。
核心发现:Fe-Spy-3CAβ是一种基于铁蛋白纳米笼的新型阿尔茨海默病疫苗,经小鼠与恒河猴实验证实,其能安全高效地清除Aβ斑块、改善记忆(雄性效果更优),突破了传统疫苗局限,为神经退行性疾病提供了通用免疫治疗新策略。
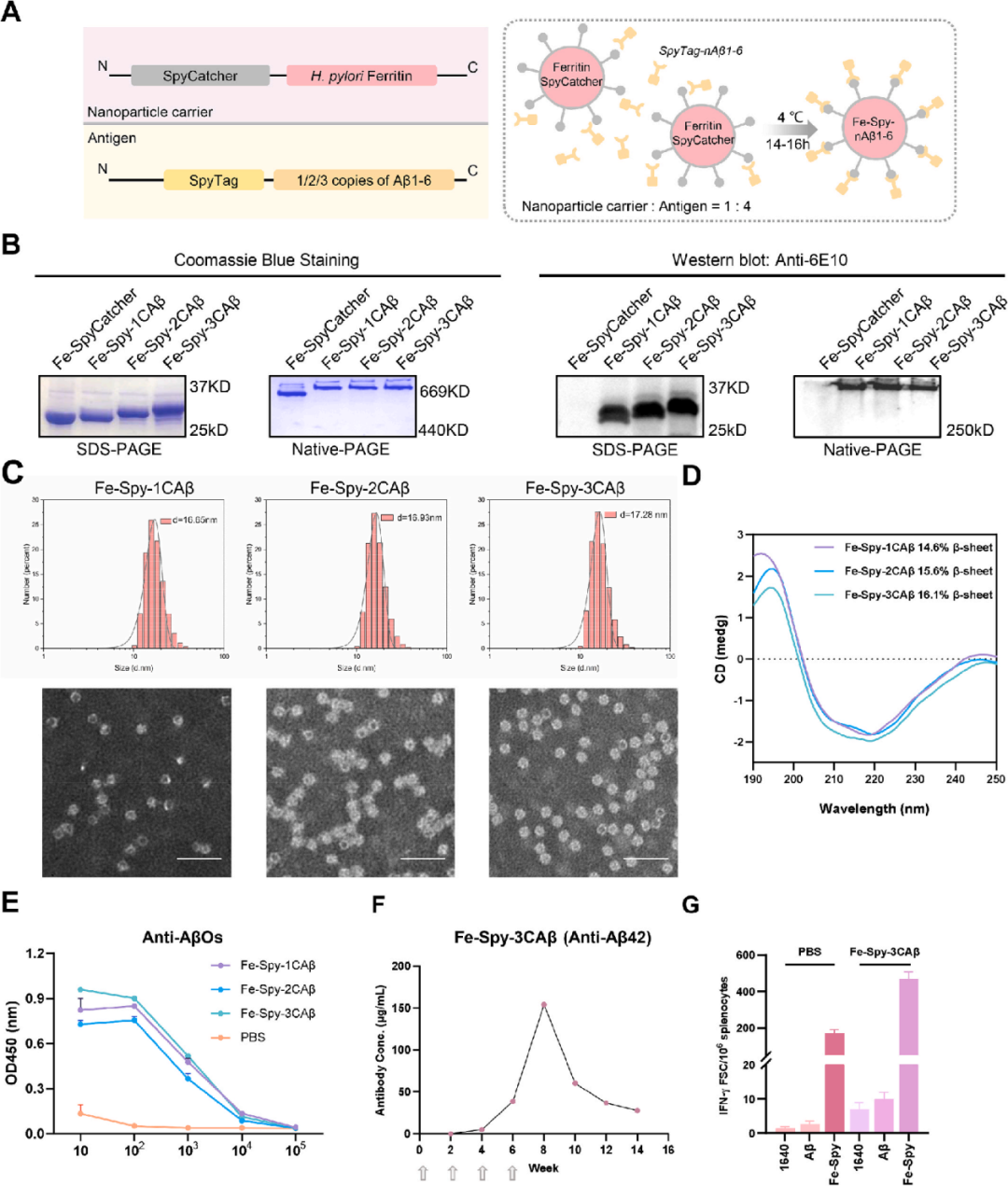
该疫苗利用“铁蛋白纳米笼”作为载体,通过“分子魔术贴”(SpyCatcher-SpyTag技术)将AD关键抗原(Aβ1-6)精准组装在表面,形成结构稳定的球形纳米颗粒。
研究发现,挂载三个拷贝抗原的构建体形成了最理想的反平行β-折叠空间结构。这种特殊的立体构象比线性序列更能模拟真实的致病寡聚体,因此诱导出的抗体特异性最强。
疫苗能诱导持久的高浓度抗体,其独特之处在于利用载体本身(铁蛋白)激发强烈的辅助T细胞反应,从而“借力”激活针对Aβ的B细胞产生高效抗体,同时避免了对Aβ自身产生过强的炎症T细胞反应。
经筛选,确定25 μg三拷贝疫苗加CpG与MF59双佐剂为肌肉注射的最佳组合,实现了安全性与免疫效果的最优平衡。
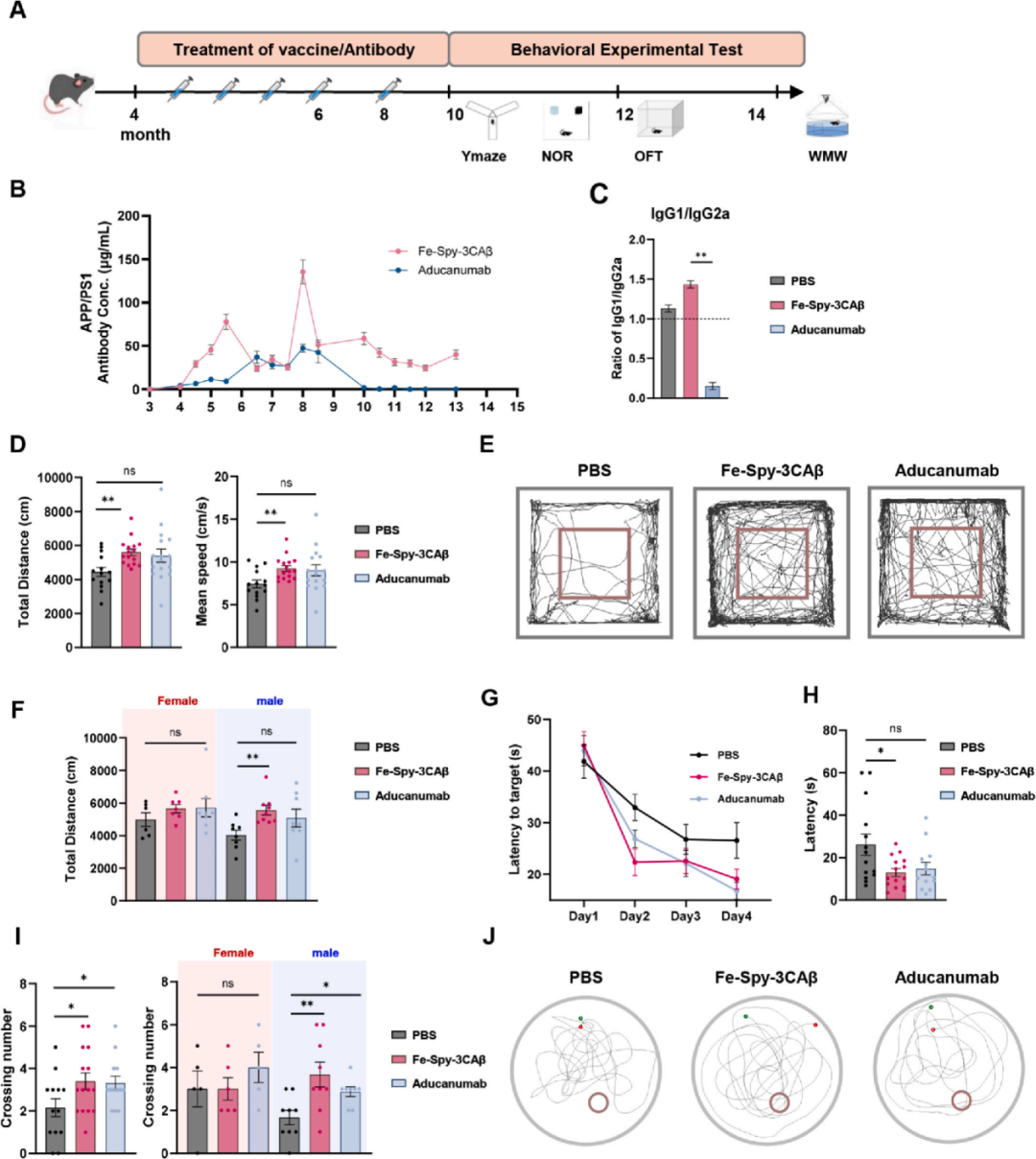
在APP/PS1阿尔茨海默病小鼠模型中,Fe-Spy-3CAβ疫苗展现出优于市售药物阿杜卡奴单抗的治疗潜力:
疫苗诱导了高滴度且持久的抗Aβ42抗体(峰值约136 μg/mL,停药后仍维持高水平),远超阿杜卡奴单抗组。
免疫反应呈Th2偏向并激发广泛的抗体亚型(含IgG3/IgM),避免了潜在的炎症风险。
疫苗有效逆转了小鼠的运动缺陷和记忆障碍。在Morris水迷宫测试中,其提升空间记忆的效果(潜伏期缩短50%、穿越平台次数增加58%)明显优于阿杜卡奴单抗。
治疗效果呈现显著的性别差异,雄性小鼠在运动功能(提升26%)和长期记忆上的改善幅度均远超雌性,提示该疫苗对雄性AD患者可能具有更佳疗效。
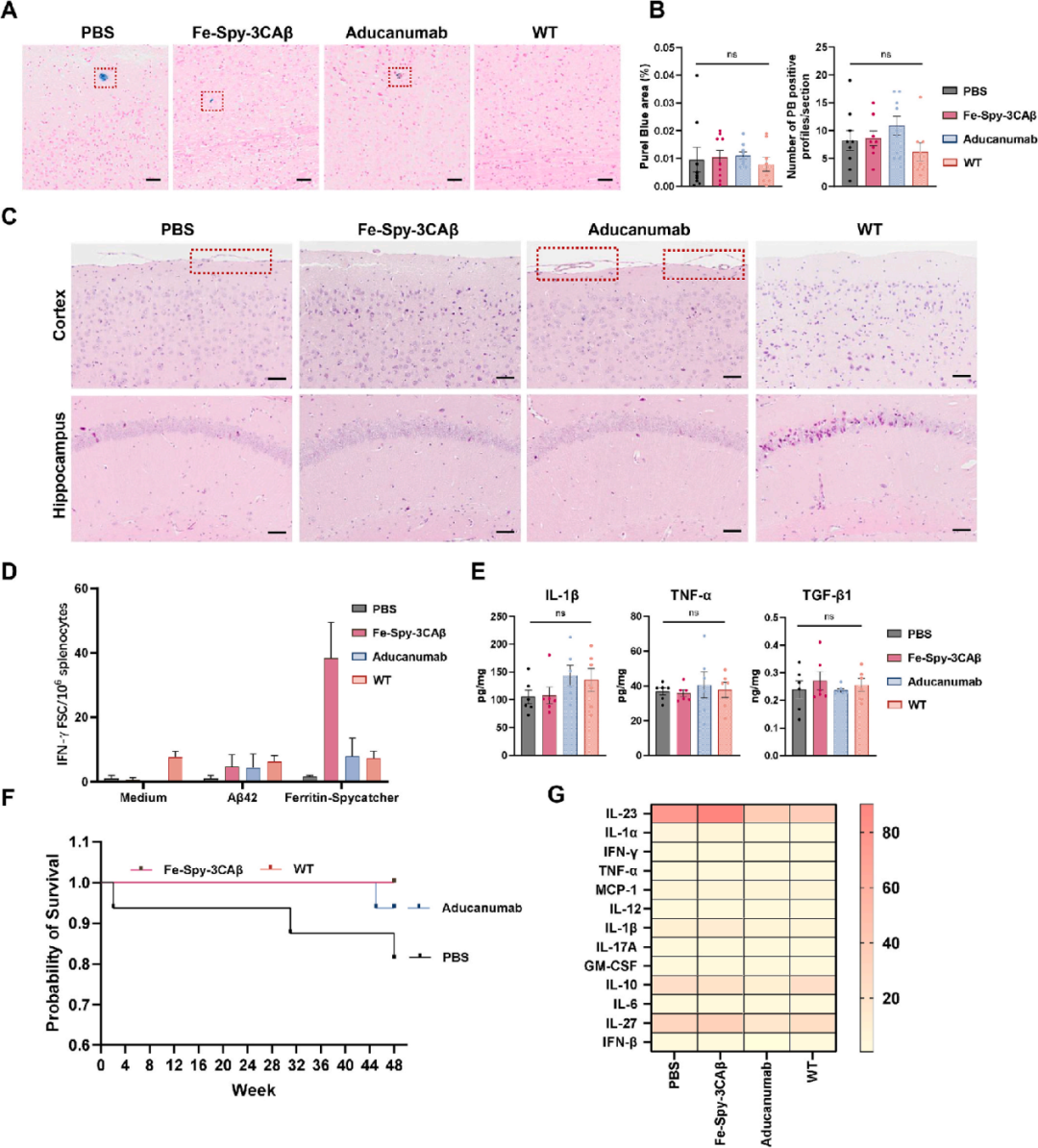
Fe-Spy-3CAβ疫苗在APP/PS1小鼠中的安全性评价
无血管毒性:普鲁士蓝染色证实未诱发微出血且H&E染色显示无单抗疗法常见的皮层隆起(血管源性水肿)及内脏病变;
免疫稳态:ELISpot与流式分析表明,疫苗未引起有害的Aβ特异性T细胞激活或神经炎症因子升高;
生存获益:相比对照组的渐进性死亡,疫苗接种显著提高了AD小鼠的存活率。
综上,该策略在避免脑出血、全身毒性及神经炎症加剧的同时,实现了优于传统单抗疗法的安全性。
它不仅克服了单抗疗法易致脑出血和水肿的安全性瓶颈,更通过诱导长效免疫实现了显著的认知改善与生存获益,为开发安全、高效且具性别特异性优势的AD预防性疫苗提供了关键转化依据。
https://doi.org/10.1016/j.bbi.2026.106486
原标题:《BBI:吉林大学吴慧团队开发新型AD纳米疫苗,让认知功能重回正轨》
 吉林大学召开领导班子树立和践行...04-05
吉林大学召开领导班子树立和践行...04-05 央视《焦点访谈》报道吉林大学第...04-05
央视《焦点访谈》报道吉林大学第...04-05 田辉到物理学院、化学学院调研04-03
田辉到物理学院、化学学院调研04-03 花开吉大 | 程立辉:用十二时辰守...04-03
花开吉大 | 程立辉:用十二时辰守...04-03 吉林大学刘雪莲教授文章入选中宣...04-02
吉林大学刘雪莲教授文章入选中宣...04-02 CCS Chemistry 2026年第4期主编寄...04-01
CCS Chemistry 2026年第4期主编寄...04-01 吉林大学召开领导班子树立和践行...03-31
吉林大学召开领导班子树立和践行...03-31 吉林大学举行2026年党员基本培训...03-31
吉林大学举行2026年党员基本培训...03-31


